Данная информация предназначена для специалистов в области здравоохранения и фармацевтики. Пациенты не должны использовать эту информацию в качестве медицинских советов или рекомендаций.
Парвовирусная инфекция В19
Ю. Б. Белан, доктор медицинских наук, профессор
М. В. Старикович, кандидат медицинских наук
ГБОУ ВПО ОмГМА МЗ РФ, Омск
В 1975 г. Yvonne Cossart, при исследовании сыворотки доноров в образце № 19
линии В, выявила парвовирус-подобные частицы, получившие название «Parvovirus
В19» [1]. Парвовирус В19 (эритровирус В19) — содержит одноцепочечную ДНК,
безоболочечный термостабильный вирус, имеющий форму двадцатигранника, диаметр
20–25 нм, принадлежит к роду Erythrovirus, семейству Parvoviridae (рис. 1).
Выделяют три генотипа: генотип 1 распространен повсеместно; генотип 2
встречается довольно редко в Европе, Бразилии, Вьетнаме, Северной Америке;
генотип 3 преимущественно регистрируется в западной Африке, спорадические случаи
зарегистрированы во Франции, Великобритании, Бразилии и Азии; в Южной Африке
регистрируются все три генотипа [2–4].
Геном парвовируса В19 кодирует: два капсидных протеина VP1 и VP2;
неструктурный протеин NS-1; малые неструктурные протеины 11-Da, 9-Da и 7,5-kDa.
Протеин NS-1 является трансактиватором вирусного Р6 промотора экспрессии
WAF1/CIP1 гена, продукт которого р21WAF ингибирует циклин-Cdk комплексы,
блокируя клеточный цикл в G1-фазу, также NS-1 нарушает функцию E2 F-семейства
транскрипциональных факторов, блокируя клеточный цикл в G2/M-фазы, что
обеспечивает репликацию вирусной ДНК [5–7]. Протеин VP2 обладает способностью к
самосборке вирусного капсида в отсутствии вирусной ДНК, с образованием частиц,
сходных по антигенным и иммуногенным свойствам с вирионом [8]. Протеин VP1
содержит подобную фосфолипазе А2 область (VP1 u), отвечающую за инвазию вируса в
ядро инфицированной клетки [9]. 11-Da протеин играет важную роль в репликации
вирусной ДНК и апоптозе инфицированных клеток [10].
Клеточным рецептором для парвовируса В19 является Р-антиген, расположенный на
клетках трофобласта, костного мозга, печени, почек, легких, синовиальной
оболочки, эпителии, эндотелии, миоцитах, лимфоидной ткани [11, 12]. Люди, у
которых отсутствует Р-антиген (1 на 200 000 человек), не восприимчивы к
парвовирусной инфекции [13]. Жизненный цикл парвовируса B19 состоит из следующих
этапов: связывание с Р-антигеном; интернализация — проникновение внутрь клетки с
помощью a5b1-интегринов; переход в ядро клетки, репликация ДНК; транскрипция,
сборка капсида; упаковка генома в капсид, лизис клетки-хозяина и выход вирионов
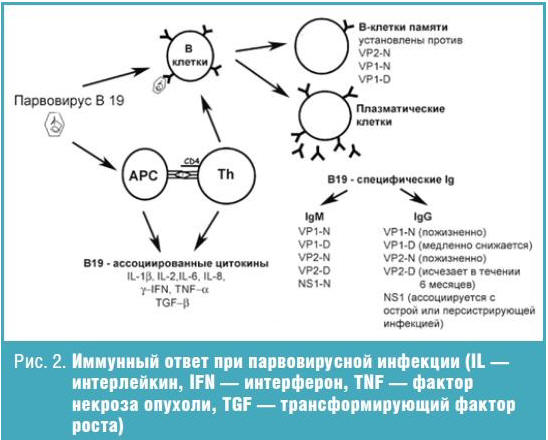
[14]. Основные компоненты клеточного и гуморального иммунного ответа на
парвовирус В19 представлены на рис. 2 [15].

Парвовирус В19 широко распространен в популяции людей, более чем 80%
взрослого населения являются серопозитивными, частота выявления IgG к
парвовирусу у детей первых десяти лет жизни составляет от 2% до 21% (рис. 3). В
25–68% случаев парвовирусная инфекция В19 протекает бессимптомно [16]. Во время
беременности к парвовирусной инфекции восприимчивы 1–5% женщин, в период подъема
заболеваемости до 3–34%, у 50% женщин парвовирусная инфекция протекает
бессимптомно [17, 18]. Максимальный уровень Р-антигена на ворсинах трофобласта
регистрируется в первом и втором триместре беременности, что определяет
трансплацентарную передачу вируса с развитием спонтанных абортов, неиммунной
водянки, внутриутробной гибели плода [19, 20].
Основной путь передачи парвовирусной инфекции В19 — воздушно-капельный, также
возможны трансплацентарный, трансфузионный, трансплантационный пути заражения
[21–23]. Характерна зимне-весенняя сезонность, с максимальным подъемом
заболеваемости в весенние месяцы. Эпидемические подъемы заболеваемости
парвовирусной инфекцией наблюдаются каждые 3–6 лет. Инкубационный период в
среднем составляет от 4 до 14 дней (максимальный до 21 дня), вирусемия
развивается приблизительно через 7 дней после инокуляции вируса и продолжается в
течение 4–7 суток [24]. Патофизиологические компоненты парвовирусной инфекции
В19 представлены на рис. 4.
Парвовирус В19 ассоциируется с разнообразными заболеваниями, развитие которых
сопряжено с особенностями иммунологического и гематологического статуса человека
(таблица).


Инфекционная эритема
Инфекционная эритема — наиболее распространенная клиническая форма
парвовирусной инфекции В19 у детей. Начинается с неспецифических симптомов —
лихорадка, недомогание, озноб, миалгии, которые продолжаются в течение 2–5
суток. Затем присоединяется патогномоничный симптом «отшлепанных» щек — яркая
эритема кожи в области щек, а также пятнисто-папулезная сыпь на туловище и
конечностях, быстро трансформирующаяся в «кружевную» сыпь, зуд не беспокоит
(рис. 5). Экзантема при парвовирусной инфекции может сохраняться до 2–3 недель,
разрешается самостоятельно, иногда отмечается усиление сыпи после «горячей»
ванны или воздействия УФ-лучей [25].

Пятнисто-папулезная эритема с синдромом «перчаток и носков»
Данная форма парвовирусной инфекции В19 характеризуется: острым началом
заболевания с повышения температуры, недомогания, головной боли, снижения
аппетита, артралгий; отеком кистей и стоп с одновременным появлением на коже
пятнисто-папулезной эритемы, в ряде случаев с геморрагическим компонентом, в
виде «перчаток и носков» (рис. 6); в полости рта на слизистой твердого и мягкого
неба, языке, губах могут формироваться эрозии [26–28]. Продолжительность
заболевания составляет 1–2 недели, разрешаются симптомы самостоятельно.

Синдром полиартропатии
Синдром полиартропатии наблюдается у 75% взрослых с инфекционной эритемой,
чаще у женщин средних лет. В процесс вовлекаются пястно-фаланговые,
лучезапястные, локтевые, коленные, голеностопные суставы. Обычно наблюдается
симметричное поражение суставов. Синдром полиартропатии клинически напоминает
ревматоидный артрит, может персистировать в течение 3 месяцев, повторяться
несколько раз в течение года [29].
Транзиторный апластический криз
Транзиторный апластический криз развивается при парвовирусной инфекции В19 у
пациентов с наследственным микросфероцитозом, серповидно-клеточной и
железодефицитной анемией, талассемией. Характеризуется не только парциальной
гипоплазией эритроидного ростка, но и развитием тромбоцитопении, нейтропении и
даже панцитопении [30, 31].
Поражение ЦНС
Неврологическая манифестация парвовирусной инфекции В19 сопровождается
развитием: энцефалита, менингоэнцефалита, судорожного синдрома, периферических
невропатий, синдрома запястного канала [32].
Поражение печени
Парвовирус В19 может вызывать острый гепатит, фульминантную печеночную
недостаточностью, хронический гепатит, гепатит-ассоциированную апластическую
анемию, гепатит с гемофагоцитарным лимфогистиоцитозом [33]. При биопсии печени
выявляется гепатоцеллюлярный и каналикулярный холестаз, апоптоз и некроз
гепатоцитов [34, 35].
Кардит
Энтеровирусы и аденовирусы до недавнего времени считались основными причинами
вирусных кардитов, однако с внедрением метода полимеразной цепной реакции с
гибридизационно-флюоресцентной детекцией, при проведении эндомиокардиальной
биопсии все чаще стали регистрироваться парвовирус В19 и вирус герпеса 6-го типа
[36]. Многочисленные копии вирусного генома парвовируса В19 определяются в
эндотелии интрамиокардиальных артериол, капилляров и посткапилярных венул,
инициируя синтез фактора некроза опухоли альфа (ФНО-a), интерлейкинов (ИЛ):
ИЛ-6, ИЛ-8, ИЛ-2, интерферона гамма (ИФН-g), рецепторов ИЛ-2 [37]. Прямое
цитопатическое действие парвовируса, апоптоз, активация врожденного и
адаптивного иммунного ответа приводят к эндотелиальной дисфункции с последующим
вентрикулярным ремоделированием и развитием дилатационной кардиомиопатии
[38–40].

Неиммунная водянка плода
Неиммунная водянка плода может развиваться при поражении парвовирусом В19
плода с гестационным возрастом 13–20 недель. Сопровождается анемией, гипоксией,
гепатитом (непосредственное повреждение гепатоцитов вирусом и опосредованное —
за счет отложения гемосидерина), кардитом, с формированием печеночной и
сердечной недостаточности. При проведении ультразвукового исследования плода
выявляется: кардиомегалия, отек грудной клетки, асцит, выпот жидкости в
плевральные полости и перикард, отек плаценты [41]. При своевременной
диагностике и проведении гемотрансфузии плоду внутриутробно, благоприятный исход
возможен в 83% случаев [42].
Врожденная парвовирусная инфекция В19
В первые месяцы жизни ребенка врожденная парвовирусная инфекция манифестирует
развитием анемии Даймонда–Блекфена, гидроцефалии, полимикрогирии, кардита,
гепатита [43, 44].
Диагностика парвовирусной инфекции В19
Гематологические изменения чаще носят преходящий характер в виде анемии,
ретикулоцитопении или полного отсутствия ретикулоцитов, нейтропении, эозинофилии,
моноцитоза, тромбоцитопении. Возможно повышение печеночных трансаминаз (аланинаминотрансферазы
и аспартатаминотрансферазы), С-реактивного белка, скорости оседания эритроцитов.
Методы диагностики парвовирусной инфекции В19:
- Полимеразная цепная реакция (ПЦР) с гибридизационно-флуоресцентной
детекцией «АмплиСенс® Parvovirus B19-FL» (сыворотка, ликвор, пунктат костного
мозга, биоптат кожи и т. д.) — определение ДНК парвовируса.
- Иммуноферментный анализ (ИФА) «Parvovirus B19 IgM/Parvovirus B19 IgG»
(сыворотка крови) — IgM в сыворотке крови пациента обнаруживаются одновременно
с появлением симптомов заболевания (на 12–14 день после заражения), их уровень
достигает максимума на 30-й день, затем снижается в течение 2–3 месяцев. Через
5–7 дней от момента клинических проявлений парвовирусной инфекции появляются
IgG, которые сохраняются в течение нескольких лет.
- Парвовирус В19 иммуноблот IgM/IgG «RIDA® Blot Parvovirus B19» (сыворотка
крови).
- Учитывая способность парвовируса В19 к изоляции в тропных структурах
(костный мозг, трофобласты) отрицательный результат ПЦР крови на парвовирус
B19 еще не означает отсутствие инфицирования, а должен рассматриваться как
возможно ложноотрицательный. Для большей диагностической информативности
следует проводить ПЦР различных материалов и в сочетании с иммуноблотом IgM/IgG.
В случае, если у беременной женщины регистрируются симптомы парвовирусной
инфекции В19 (инфекционная эритема, артропатии) или она была в контакте с
больным данной инфекцией, рекомендовано проведение ПЦР и/или ИФА сыворотки
крови. При выявлении IgM к парвовирусу или положительном результате ПЦР
необходимо УЗИ плода каждые 2 недели. При наличии УЗ-признаков неиммунной
водянки плода показано проведение кордоцентеза или амниоцентеза (ПЦР крови плода
или амниотической жидкости на парвовирус В19) [45]. При положительных данных на
парвовирус B19 и ультразвуковых признаках поражения плода ставится вопрос о
прерывании беременности.
Терапия парвовирусной инфекции В19
В настоящее время специфической этиотропной терапии парвовирусной инфекции не
существует. В зависимости от клинической формы парвовирусной инфекции В19
проводится посиндромная терапия (нестероидные противовоспалительные препараты,
глюкокортикостероидные препараты, трансфузия эритромассы и т. д.). При поражении
нервной системы, кардите, гепатите — внутривенный человеческий иммуноглобулин.
Наиболее эффективны препараты иммуноглобулина, полученные от большого числа
доноров: Октагам, Интраглобин, Пентаглобин.
Профилактика парвовирусной инфекции В19
Эффективной профилактики парвовирусной инфекции в настоящее время не
существует. Ведется разработка безопасной и иммуногенной вакцины против
парвовирусной инфекции В19 [46].
Основные меры профилактики направлены на предотвращение внутриутробного
инфицирования плода: введение скрининга до планируемой беременности и во время
беременности на наличие IgG к парвовирусу В19; информирование серонегативной
беременной женщины о существовании парвовирусной инфекции В19, а также о
необходимости ограничения контакта с детьми, особенно с типичными проявлениями
парвовирусной инфекции [47].
В заключение необходимо отметить, что в нашей стране не ведется статистика
заболеваемости парвовирусной инфекцией В19, а также нет точных данных о случаях
врожденной парвовирусной инфекции. Наш опыт свидетельствует, что в ряде случаев,
при клинических проявлениях врожденной инфекции, парвовирус B19 может
ассоциироваться в частности с герпесвирусами, что существенно затрудняет как
диагностику, так и лечение данных пациентов. Учитывая это, следует признать
рациональным включение обследования на парвовирус В19 новорожденных детей при
подозрении на врожденную инфекцию.
Литература
- Cossart Y. E., Field A. M., Cant B. et al. Parvovirus-like
particles in human sera // Lancet. 1975; 1: 72–73.
- Servant A., Laperche S., Lallemand F. et al. Genetic diversity
within human erythroviruses: identiication of three genotypes // Journal of
Virology. 2002; 76 (18): 9124–9134.
- Candotti D., Etiz N., Parsyan A., Allain J.-P. Identification and
characterization of persistent human erythrovirus infection in blood donor
samples // J Virol. 2004; 78: 12169–12178.
- Corcoran C., Hardie D., Yeats J., Smuts H. Genetic variants of
human parvovirus B19 in South Africa: cocirculation of three genotypes and
identification of a novel subtype of genotype 1 // J Clin Microbiol. 2010; 48:
137–142.
- Zhi N., Mills I. P., Lu J. et al. Molecular and functional
analyses of a human parvovirus B19 infectious clone demonstrates essential
roles for NS1, VP1, and the 11-kilodalton protein in virus replication and
infectivity // J. Virol. 2006; 80: 5941–5950.
- Nakashima A., Morita E., Saito S., Sugamura K. Human Parvovirus
B19 nonstructural protein transactivates the p21/WAF1 through Sp1 // Virology.
2004; 329 (2): 493–504.
- Wan Z., Zhi N., Wong S. et al. Human parvovirus B19 causes cell
cycle arrest of human erythroid progenitors via deregulation of the E2 F
family of transcription factors // J. Clin. Invest. 2010; 120: 3530–3544.
- Kaufmann B., Chipman P. R., Kostyuchenko V. A. et al.
Visualization of the externalized VP2 N termini of infectious human parvovirus
B19 // J. Virol. 2008; 82: 7306–7312.
- Zadori Z., Szelei J., Lacoste M. C. et al. A viral phospholipase
A2 is required for parvovirus infectivity // Dev. Cell. 2001; 1: 291–302.
- Chen A. Y. et al. The small 11 kDa non-structural protein of
human parvovirus B19 plays a key role in inducing apoptosis during B19 virus
infection of primary erythroid progenitor cells // Blood. 2010; 115:
1070–1080.
- Brown K. E., Anderson S. M., Young N. S. Erythrocyte P antigen:
cellular receptor for B19 parvovirus // Science. 1993; 262: 114–117.
- Cooling L. L., Koerner T. A., Naides S. J. Multiple
glycosphingolipids determine the tissue tropism of parvovirus B19 // J Infect
Dis. 1995; 172: 1198–1205.
- Brown K. E., Hibbs J. R., Gallinella G. et al. Resistance to
parvovirus B19 infection due to lack of virus receptor (erythrocyte P antigen)
// NEJM. 1994; 330: 1192–1196.
- Servant-Delmas A., Lefrere J. J., Morinet F. et al. Advances in
human B19 erythrovirus biology // J Virol. 2010; 84: 9658–9665.
- Corcoran A., Doyle S. Advances in the biology, diagnosis and host–pathogen
interactions of parvovirus B19 // Journal of Medical Microbiology. 2004; 53:
459–475.
- Noyola D. E., Lourdes Padilla-Ruiz M., Guadalupe Obregón-Ramos M.
et al. Parvovirus B19 infection in medical students during a hospital outbreak
// J Med Microbiol. 2004; 53: 141–146.
- Feldman D. M., Timms D., Borgida A. F. Toxoplasmosis, parvovirus,
and cytomegalovirus in pregnancy // Clin Lab Med. 2010; 30 (3): 709–720.
- Tolfvenstam T., Broliden K. Parvovirus B19 infection // Semin
Fetal Neonatal Med. 2009; 14 (4): 218–221.
- Jordan J. A., DeLoia J. A. Globoside expression within the human
placenta // Placenta. 1999; 20: 103–108.
- Public Health Laboratory Service Working Party on Fifth Disease.
Prospective study of human parvovirus infection in pregnancy // Br Med J.
1990; 300: 1166–1170.
- Jordan J., Tiangco B., Kiss J., Koch W. Human parvovirus B19:
prevalence of viral DNA in volunteer blood donors and clinical outcomes of
transfusion recipients // Vox Sang. 1998; 75: 97–102.
- Cohen B. J., Beard S., Knowles W. A. et al. Chronic anemia due to
parvovirus B19 infection in a bone marrow transplant patient after platelet
transfusion // Transfusion. 1997; 37: 947–952.
- Lamont R. F., Sobel J., Vaisbuch E. et al. Parvovirus B19
infection in human pregnancy // BJOG. 2011; 118 (2): 175–186.
- Van Beers-Tas M. H., Heidema J. Review: Pathogenesis of
parvovirus infections in children // Virol Mycol. 2013; 2 (1): 110.
- Anderson L. J. Role of parvovirus B19 in human disease // Pediatr.
Infect. Dis. 1987: 6: 711–718.
- Valentin M. N., Cohen P. J. Pediatric Parvovirus B19: spectrum of
clinical manifestations // Cutis. 2013; 92: 179–184.
- Pavlovic M. D. Papular-purpuric «gloves and socks» syndrome
caused by parvovirus B19 // Vojnosanit Pregl. 2003; 60 (2): 223–225.
- Heckler G. T., Dal Ri N. M. K., Almeida H. L. Jr. Case for
diagnosis // An Bras Dermatol. 2012; 87 (5): 793–794.
- Kumano K. Various clinical symptoms in human parvovirus B19
infection // Japanese Journal of Clinical Immunology. 2008; 31 (6): 448–453.
- Muir K., Todd W. T., Watson W. H., Fitzsimons E. Viral-associated
haemophagocytosis with parvovirus-B19-related pancytopenia // Lancet. 1992;
339: 1139–1140.
- Saarinen U. M., Chorba T. L., Tattersall P. et al. Human
parvovirus B19-induced epidemic acute red cell aplasia in patients with
hereditary hemolytic anemia // Blood. 1986; 67: 1411–1417.
- Douvoyiannis M., Litman N., Goldman D. L. Neurologic
manifestations associated with Parvovirus B19 Infection // CID. 2009; 48 (15):
1713–1723.
- Bihari Ch., Rastogi A., Saxena P. et al. Parvovirus B19
associated hepatitis // Hindawi Publishing Corporation // Hepatitis Research
and Treatment. 2013; Article ID 472027: 1–9.
- Poole B. D., Karetnyi Y. V., Naides S. J. Parvovirus B19-induced
apoptosis of hepatocytes // Journal of virology. 2004; 78 (14): 7775–7783.
- Hatakka A., Klein J., He R. et al. Acute hepatitis as a
manifestation of parvovirus B19 infection // Journal of Clinical Microbiology.
2011; 49 (9): 3422–3424.
- Kindermann I., Barth C., Mahfoud F. et al. Update on Myocarditis
// Journal of the American College of Cardiology. 2012; 59 (9): 779–792.
- Klingel K., Selinka H.-C., Sauter M. et al. Molecular mechanisms
in enterovirus and parvovirus B19 associated myocarditis and inflammatory
cardiomyopathy // European Heart Journal. 2002; 4 (1): 108–112.
- Schultheiss H.-P., Kuhl U., Cooper L. T. The management of
myocarditis // European Heart Journal. 2011; doi: 10.1093: 1–13.
- Caforio A. L. P., Bottaro S., Iliceto S. Dilated cardiomyopathy (DCM)
and myocarditis: classification, clinical and autoimmune features // Applied
Cardiopulmonary Pathophysiology. 2012; 16: 82–95.
- Santos Tavares P., Rocon-Albuquerque R., Leite-Moreira A. F.
Innate immune receptor activation in viral myocarditis: pathophysiologic
implications // Rev Port Cardiol. 2010; 29 (01): 57–78.
- Smith J. Human parvovirus B19: a literature review and case study
// Infant. 2008; 4 (5): 101–104.
- Ergaz Z., Ornoy A. Parvovirus B19 in pregnancy // Reproductive
Toxicology. 2006; 21: 421–435.
- Giorgio E., Antonietta De Oronzo M., Iozza I. Parvovirus B19
during pregnancy: a review // Journal of Prenatal Medicine. 2010; 4 (4):
63–66.
- Schulert G. S., Walsh W. F., Weitkamp J. H. Polymicrogyria and
congenital Parvovirus B19 infection // Am J Perinatol Rep. 2011; 1: 105–110.
- Dieck D., Schild R. L., Hansmann M., Eis-Hubinger A. M. Prenatal
diagnosis of congenital parvovirus B19 infections: value of serological and
PCR techniques in maternal and fetal serum // Prenatal Diagnosis. 1999; 19:
1119–1123.
- Bernstein D. I., Sahly H., Keitel W. A. et al. Safety and
immunogenicity of a candidate Parvovirus B19 vaccine // Vaccine. 2011; 29
(43): 7357–7363.
- Pickering L. K., Baker C. J., Kimberlin D. W. et al. Parvovirus
B19. Report of the Committee on Infectious Diseases // American Academy of
Pediatrics. 2009: 491–494.
Статья опубликована в журнале
Лечащий Врач

